| | transition dipolaire |  |
|
|
|
| Auteur | Message |
|---|
jfcp
Irrécupérable

Nombre de messages : 673
Age : 39
Localisation : forest (aime tjs pas bxl ;-)
Date d'inscription : 01/02/2005
 |  Sujet: transition dipolaire Sujet: transition dipolaire  Mar 27 Déc - 12:20 Mar 27 Déc - 12:20 | |
| c'est quoi cette bête là??
et puisquelqu'un a compris ces trucs sur l'atome de carbone:
L=0 et 2 est pair tandis que L=1 est impair.
pourqoui c'est L=1 et S=1 qui serait le fondamental (pourqoui lui et pas un autre?)
bref je patauge, je vois rien d'équivalent ds le merschbaker.... | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 27 Déc - 12:45 Mar 27 Déc - 12:45 | |
| L = 0 et 2 est pair et L = 1 est impaire car les fonction propre sont proportionelle au harmonique spherique Ylm et que P Ylm = -1^l Ylm S = 0 est impaire et S = 1 est pair car la fonction propre de S = 0 c'est ( 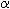 1 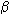 2 - 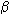 1 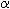 2)/2 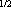 qui est donc impaire sous paritée! pour dire que S = 1 L = 1 est le fondamentale, il faut faire une experience, on ne sias pas le calculer... c'est souvent l'état qui minimine l'énergie, plus précisement celui qui minimise le couplage spin orbite..., mais c'est pas toujours le cas, car il y a parfois des effet plus important qui joue... en bref, on ne peux pas dire qu'elle est le vrai état fondamentale sans faire d'experience... PS : la transition bipolaire electrique c'est quand un atome exitée retombe a un niveau plus bas, en lachant des photons, mais ca tu le savais déja  au plaisir  | |
|
  | |
jfcp
Irrécupérable

Nombre de messages : 673
Age : 39
Localisation : forest (aime tjs pas bxl ;-)
Date d'inscription : 01/02/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 13:09 Mer 28 Déc - 13:09 | |
| Bon l’histoire de la symétrie, j’ai compris  (un peu longue à la détente parfois mais c pas grave..) Si on admet que l’amplitude de transition est bien donnée avec le D moment dipolaire électrique au milieu de braket ( pas le temps de chercher d’ou ca vient de toute façon), je vois bien qu’il faut que les états finaux et initiaux aient une parité différente, cette parité dépendant forcément du « l » de l’état par définition. Après pour l’hydrogène on peut donc passer de l’état (2P) à l’état (2S) par transition dipolaire. Weyers demande de calculer l’énergie du photon et sa longueur d’onde. Naïvement l’énergie du photon c’est bien -13,6/4 +13,6 = 3*13,6/4 ev et je trouve alors une longueur d’onde de 122 nm (pas dans le visible donc), comme l’ordre de grandeur (nm) me paraît réaliste, pourquoi pas ….mais devait on tenir compte d’un éventuel effet spin orbite, ca m’embrouille à la fin ce truc… Mais alors il faut faire la même chose pour le sodium dont le dernier électron passe de (3P) à (3S), comme c’est le même n dans les deux cas il faut tenir compte de l’effet spin orbite pour que ces deux niveaux n’aient pas la même énergie… (3S) : l=0, S=1/2 , J= 1/2 , L*S=1/2 * (1/2*(1/2+1)-0(0+1)-1/2*(1/2+1))=0 (3P) : l=1, S=1/2 , J= 3/2 (ou 1/2) , L*S=1/2 * (3/2*(3/2+1)-1(1+1)-1/2*(1/2+1))=0,5 ou L*S=1/2 * (1/2*(1/2+1)-1(1+1)-1/2*(1/2+1))= -1 dans tout les cas je trouve pas le 2,5 donné par weyers au cours. Ce 2,5 étant logique car il donne bien une longueur d’onde dans le jaune… je me trompe donc quelque part (ou alors j’ai rien compris  ) | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 14:16 Mer 28 Déc - 14:16 | |
| heu...
effectivement ca foire....
parcontre si tu fais 3p -> 2s ca marche a peut pres
je trouve 2.4
peut etre c'est t'il trompé? c'est juste une suggestion...
EDIT : JE NE TROUVE PAS 2.4, jme suis planté
Dernière édition par le Mer 28 Déc - 16:06, édité 1 fois | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 15:21 Mer 28 Déc - 15:21 | |
| Bonjour à tous! Je pense que quelques mises au point s'imposent (ca fait un peu sévère comme entrée en matière, désolé!) 1)Pour bien situer le débat, nous parlons ici d'interaction onde electromagnétique (perturbation dépendant du temps) - atome (systeme quantique). Cela va nous permettre d'étudier les phénomène d'absorption et d'émission de radiation. Pour un développement de base, cfr http://farside.ph.utexas.edu/teaching/qm/perturbation/node17.htmlSi l'on ne prend le premier terme (1) du developpement de l'exp de l'eq 259 (en supposant donc le rapport 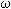 /c est petit, c'est à dire que la longueur d'onde de l'onde EM est bcp plus grande que la taille de l'atome), cfr http://farside.ph.utexas.edu/teaching/qm/perturbation/node18.htmlon simplifie grandement le problème. Cela s'appelle faire "l'approximation dipolaire électrique" Cela revient à ne considérer qu'une sous-classe des phénomènes d'absorption/émission appelées les "transitions dipolaires". Il faut être conscient du fait que d'autres types de transitions existent (ex: transition magnétique dipolaire (10^5 fois moins probables) ou quadrupolaire électrique (obtenue avec le second terme de l'exp, 10^8 fois moins probables) ). J'espère que la notion est plus claire maintenant. 2) Pour chaque type de transition, il existe des "rêgles de sélection" souvent justifiées par des raisons de symétries. Dans le cas des transitions dipolaires électriques il s'agit de :gdelta:l=+-1 et :gdelta:m=0,+-1 (cfr. http://farside.ph.utexas.edu/teaching/qm/perturbation/node18.html pour une explication). Une transition dipolaire peut donc avoir lieu entre 2p et 1s (:gdelta:l=1) mais pas entre 2s et 1s (:gdelta:l=0). 3) Puisque :gdelta:l=+-1, il faut en effet une levée de dégéneresence entre niveaux de même n et de l différents pour observer des transitions de type nP->nS (jfcp, ton premier calcul de 122nm (10eV) correspond à une (bonne) approximation de la transition 2p->1s de l'H, pas 2p->2s qui naivement donne 0). Dans le cas de l'H, le couplage spin-orbite mène à une levée de dégénerescence (differentes E pour différent j, au sein d'un même l) mais certainement pas assez pour observer 2p->2s (le photon aurait une energie ~10^-5eV!). Par contre on peut voir l'effet en comparant 2p(1/2)->1s et 2p(3/2)->1s: apparition d'une double raie dans le spectre -> le nom de "structure fine". Le mécanisme qui provoque la levée de dégénérescence 3s/3p dans le Na (et 2p/2s dans le Li) n'a rien à voir! Si on modélise ces atomes comme des Hydrogenoides, en supposant que les couches electroniques remplies (n=1 pour Li, n=1 et n=2 pour Na) écrantent completement les protons du noyeau correspondant, on ne s'attend pas à observer de difference qualitative avec le spectre de H. Mais dans la réalité, un électron de la couche externe S (2s pour Li, 3s pour Na) "rentre" plus dans la couche interne 1s qu'un electron dans la couche externe P. L'écrantage est donc moins fort et l'electron S est plus lié que le P -> levée de dégénrescence entre S et P -> transition dipolaire entre niveau de même n possible. Le calcul quantitatif me semble par contre a priori non trivial et je voudrai savoir si Mr Weyers vous l'a réellement donné en exercice. Voilà, j'espère que cela répond à un maximum de questions! Un dernier lien, "pour la route", http://hyperphysics.phy-astr.gsu.edu/hbase/hframe.htmlAllez jetter un coup d'oeil à la partie Atomic properties pour une belle série de graphe illustrant ces explications... Bon bloc & courage Michel PS: Pour cette réponse, et pour celles éventuellement à venir j'espère que je ne m'éloigne pas trop du cours de Mr Weyers, que je n'ai malheureusement pas suivi... | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 15:50 Mer 28 Déc - 15:50 | |
| bhen en faite weyers n'as pas introduit les transition dipolaire car il les supose connues... (j'imagine qu'on les verra au prochain quadri...) donc c'ets des lors assez dur... pour cet exemple la, il a juste dis : pour le sodium, la config electronique est (Ne)(3S) quand l'atome est exitée la config devient (Ne)(3P) et l'atome se désexite par l'emission d'un photon (Ne)(3P) -> (Ne)(3S) + 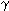 (de 2.5ev) la question est donc... comment trouve t'il 2.5ev? mais pour moi, on ne peut pas avoir (Ne)(3P) -> (Ne)(3S) pas avec une transition dipolaire en tout cas, car on ne respecte pas les regle de selection, qui sont paritée inverse et difference de niveau d'energie de 1 c'ets pourquoi, je pense que on devrait avoir (Ne)(3P) -> (Ne)(2S) | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 16:09 Mer 28 Déc - 16:09 | |
| Et la réponse est: difficilement...
L'étude générale d'un atome complexe comme le sodium est impossible analytiquement, hors on ne peut pas se contenter ici de l'approximation hydrogénoide. Je présume que l'on peu appliquer une formule empirique ou l'autre (eventuellement issue de l'étude des perturbations pour des atomes plus simples, comme l'He que l'on a vu ensemble) mais n'en sais pas plus et je doute fortement que vous soyez supposés pouvoir calculer ce nombre. Je peux éventuellement en toucher un mot à Mr Weyers la semaine prochaine si vous le desirez...
Sinon, en ce qui concerne les transitions dipolaires en général je pense que le premier lien de mon post précédent se suffit à lui-même pour une première approche.
A bientot,
EDIT: Loicus, pour la suite de ton post, je maintiens que l'on peut avoir 3P->3S (cfr mon dernier lien pour vérifier). :gdelta:n=1 n'est pas une rêgle de sélection. 3P->2S est même interdit par le principe de Pauli pour l'électron externe puisque la couche n=2 est déja remplie dans le Na... En d'autre mot, le fondamental de Na, c'est 3S, pas 2S (11 e-, 2 sur 1s, 2 sur 2s et 6 sur 2p, et 1 sur 3s)
Dernière édition par le Mer 28 Déc - 16:20, édité 3 fois | |
|
  | |
jfcp
Irrécupérable

Nombre de messages : 673
Age : 39
Localisation : forest (aime tjs pas bxl ;-)
Date d'inscription : 01/02/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 16:11 Mer 28 Déc - 16:11 | |
| bon ben je vais regarder tout ca
en tout cas a grand merci | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 17:10 Mer 28 Déc - 17:10 | |
| oui de faite... merci michel... par contre encore une mini question a ce sujet on a vu au cour que pour l'atome d'hydrogene N=3 les désintégration possible sont 3S -> 2P 3P -> 2S 3D -> 2P 2P -> 1S si les regles de selection sont : gdelta: l = 1 et paritée différente pour quoi ets ce qu'on as pas? 3P -> 1S (c'ets pour ca que j'avais déduit  N = 1 sans bonne raison, je l'avoue  ) merci d'avance | |
|
  | |
jfcp
Irrécupérable

Nombre de messages : 673
Age : 39
Localisation : forest (aime tjs pas bxl ;-)
Date d'inscription : 01/02/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 17:25 Mer 28 Déc - 17:25 | |
| - Citation :
- jfcp, ton premier calcul de 122nm (10eV) correspond à une (bonne) approximation de la transition 2p->1s de l'H, pas 2p->2s qui naivement donne 0
oui faute d'inattention  sinon je suppose que dasn ce le "2,5" il a du le donner pour notre info personnelle... | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 17:48 Mer 28 Déc - 17:48 | |
| Loicus, à mon avis, le problème est simplement que ta liste n'est pas exhaustive... Pour une liste complète: http://www.ioffe.rssi.ru/astro/QC/CMBR/sp_tr.html(troisième table) On voit bien que 3p->1s est possible, même plus probable que 3p->2s... Michel | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 28 Déc - 18:21 Mer 28 Déc - 18:21 | |
| ha ok... nikel, merci encore... PS : Weyers avait pas parlé de ca au cours... ca m'éclaire mieu  | |
|
  | |
Philippe
Complètement givré

Nombre de messages : 570
Localisation : Ben ça dépend...
Date d'inscription : 08/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Ven 30 Déc - 16:59 Ven 30 Déc - 16:59 | |
| Voilà en fait, si on calcul l'effet stark pour l'hydrogène avec n=2 on trouve que l'energie de deux états est modifiée 200 et 210. On trouve alors les nouveau états propre de l'hamiltonien
ie (200+210)/sqrt(2) et (200-210)/sqrt(2) Mais étant donner que ces une somme d'états de parité différente comment savoir si une transition dipolaire est possible?
je me dit qu'il suffirait de calculer
<nlm|r|200+/-210>=<nlm|r|200>+/-<nlm|r|210> mais est)ce que ces correcte? Parce que je ne voit pas comment s'assurer que le changement de parité est bien là (cfr règle de sélection).
Merci | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 4 Jan - 14:23 Mer 4 Jan - 14:23 | |
| je me pose la meme question...
on montre facilement que nos 2 nouveau état sont de paritée diff...
car P(200 + 210) = 200 - 210 notre autre état...
mais comment calculer leur paritée par rapport au état classique...? | |
|
  | |
cyrano
Chapelier fou

Nombre de messages : 170
Localisation : Wouf!
Date d'inscription : 16/06/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 4 Jan - 15:08 Mer 4 Jan - 15:08 | |
| peut-etre que tout ce qu'on peut dire, c'est qu'une transition interdite avant, est possible avec une certaine proba car "contaminée" par l'autre état dont le transition est permise... | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mer 4 Jan - 16:03 Mer 4 Jan - 16:03 | |
| et je dirais aussi que une transition est possible entre nos 2 nouveau état...
non? | |
|
  | |
cyrano
Chapelier fou

Nombre de messages : 170
Localisation : Wouf!
Date d'inscription : 16/06/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Lun 16 Jan - 20:14 Lun 16 Jan - 20:14 | |
| quelqu'un en sait plus finalement sur les transitions partant du nouvel état combili de |2 1 0> et |2 0 0> ? | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Lun 16 Jan - 21:29 Lun 16 Jan - 21:29 | |
| | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 11:14 Mar 17 Jan - 11:14 | |
| Cohen complément EXII, remarque à la fin:
W_s ayant un élément de matrice non-null entre 2s et 2p, tout champ électrique "contamine" l'état métastable 2s par l'état instable 2p (qui lui peut se désexciter par transition dipolaire vers 1s) et confère à l'état 2s une durée de vie bcp plus courte que si E=0. Ce phénomène est appelé "quenching de métastabilité. Expérimentalement, la raie correspondant à la transition 2p-1s se scindent en deux raies correspondant à la transition des états mixtes 2p/2s (qui n'ont pas la même énergie) vers 1s.
Il me semble que c'est ce que j'avais expliqué hier mais peut être est-ce plus clair maintenant ? | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 11:39 Mar 17 Jan - 11:39 | |
| je n'était pas la hier... autre mini question.... je vien de lire le complement du cohen que tu as indiqué... qui ets tres bien expliqué... il dise que 2s -> 1s en émetant 2 photon... (cependant une transition dipolaire entre ces 2 état n'est pas possible) donc j'imagine que cela ce fait via un autre type de transition... je comprend bien que le temp de vie de l'état 2s est diminué, étant donné qu'il est mixé avec du 2p qui a un temp de vie tres cours... mais la question est tjrs la meme en faite... est ce que les état mixte retombe ds le fondamental par une transition dipolaire, ou bien c'est pas un autre type de transition? (étant donné que 2p retombe vers 1s par transition dipolaire et que 2s retombe vers 1s via une autre transition) encore merci pour ton aide... EDIT : encore une autre question 3p -> 3s est possible via une transition dipolaire car  l = +-1 et  m = +-1,0 pourquoi n'est t'il pas repris ici dans le site que tu as donné la fois passé??? http://www.ioffe.rssi.ru/astro/QC/CMBR/sp_tr.html
Dernière édition par le Mar 17 Jan - 12:29, édité 1 fois | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 12:25 Mar 17 Jan - 12:25 | |
| Désolé, mais entre les noms et les surnoms je m'y perd un peu et je ne sais donc pas qui était là  En effet, lorsque le champ E=0 (avt effet Stark), 2s->1s est interdit en dipolaire électrique mais, comme mentionné dans le Cohen, la transition peut se faire dans un autre régime (par exemple quadrupolaire électrique) mais est bcp moins probable (un facteur 10^8!). Des que le champ électrique est allumé, les niveaux se mélangent et les niveaux mixtes contiennent chacun du 2p et ils peuvent tous les deux etre le point de départ d'une transition dipolaire vers 1s. Ces deux transitions entre niveaux d'énergie légerement différents (les niveaux mixtes, séparé par un gap linéaire en E -> effet stark linéaire) vers un même niveau (1s, qui n'est modifié qu'au second ordre du champ) donnent une double raie dans le spectre, dont la séparation est prop à E. Pour une illustration graphique (pour l'He, qui est un peu différent mais l'idée est là): http://hyperphysics.phy-astr.gsu.edu/hbase/atomic/stark.html#c1Voilà, j'espère que ca t'aidera... | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 12:29 Mar 17 Jan - 12:29 | |
| arg... j'ai fait un edit pdt ton post je sais pas si tu as vu
sinon ta réponse est nikel...
merci beaucoup | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 13:11 Mar 17 Jan - 13:11 | |
| Ben si tu parles de 3p->3s dans l'atome d'H "basique", ils ont le même niveau d'énergie donc le photon a une energie nulle donc une longueur d'onde infinie donc ... c'est mal barré pour le voir  Si tu ajoute des effets pour lever la dégénerescence (spin orbite, stark, ...) tu peux avoir une petite différence d'énergie mais qui ne mènera jamais à un photon observable (du moins si tu observes dans la région du visible, parce qu'il s'agit de lg d'ondes typiquement de l'ordre du m)! Ce que tu peux observer, par contre, c'est des petites différences d'énergie entre deux transitions (c'est comme ca qu'on met en évidence ces effets de structure fine). Par exemple tu ne risque pas de voir mixte1->mixte2, même après levée de dégenerescence, mais tu peux voir que mixte1 ->1s et mixte2->1s n'ont pas tout à fait la même énergie. Je ne sais pas si c'est clair... | |
|
  | |
loicus
Irrécupérable

Nombre de messages : 1453
Age : 38
Localisation : 50°40'45.01"N 4°33'19.93"E
Date d'inscription : 09/01/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 15:12 Mar 17 Jan - 15:12 | |
| oui jme disais bien que y avait un truc du genre...
parcontre c'est possible avec des atomes plus complexe que l'hydrogene, car il y a le phénomène d'écrantage qui fait qu'il y a une différence d'énergie entre les état de meme énergie mais de l différent...
j'ai bien capté?
en tout cas nikel...
je commence a bien cernée la bête
merci | |
|
  | |
Michel
Névrosé
Nombre de messages : 37
Localisation : Eghezee (ex-Montois)
Date d'inscription : 21/05/2005
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  Mar 17 Jan - 15:31 Mar 17 Jan - 15:31 | |
| Tu as bien capté  Pour etre précis c'est le fait que l'écrantage est plus effectif pour 3p que 3s qui fait que l'electron est plus attiré et donc le niveau 3s plus bas... | |
|
  | |
Contenu sponsorisé
 |  Sujet: Re: transition dipolaire Sujet: Re: transition dipolaire  | |
| |
|
  | |
| | transition dipolaire |  |
|
